Организация заключила договора поставки продукции
Главная \ Бесплатные консультации \ Бухгалтерский учет \ Организация заключила договора поставки продукции — с поставщиком и с заказчиком. Организация доставляет продукцию собственным транспортом заказчику. Как правильно заполнить строку «Пункт погрузки»?
Напряженный график не позволяет посещать мероприятия по повышению квалификации?
Мы нашли выход!
|
Консультация предоставлена 06.12.2016 года
Организация заключила два договора поставки продукции — с поставщиком и с заказчиком. При этом организация доставляет продукцию собственным транспортом заказчику с производственной площадки (склад) поставщика (Вологодская область).
Как правильно заполнить строку «Пункт погрузки» товарно-транспортной накладной?
Рассмотрев вопрос, мы пришли к следующему выводу:
В строке «Пункт погрузки» следует указывать тот адрес, с которого фактически происходит отгрузка продукции (т. е. адрес производственной площадки поставщика в Вологодской области).
е. адрес производственной площадки поставщика в Вологодской области).
Обоснование вывода:
Как правило, движение товара от поставщика к покупателю оформляется товаросопроводительными и транспортными документами, предусмотренными условиями поставки товаров и правилами перевозки грузов, в частности товарной накладной по форме N ТОРГ-12, утвержденной постановлением Госкомстата России от 25.12.1998 N 132 (далее — Постановление N 132), товарно-транспортной накладной (ТТН) по форме N 1-Т (при автомобильных перевозках), утвержденной постановлением Госкомстата России от 28.11.1997 N 78 (далее — Постановление N 78), транспортной накладной по форме, установленной Приложением N 4 к Правилам перевозки грузов автомобильным транспортом (далее — Правила), утвержденным постановлением Правительства РФ от 15.04.2011 N 272 (далее — транспортная накладная).
Следует учитывать, что в настоящее время обязательными к применению продолжают оставаться формы документов, используемых в качестве первичных учетных документов, установленные уполномоченными органами в соответствии и на основании других федеральных законов (информация Минфина России от 04. 12.2012 N ПЗ-10/2012), а формы первичных учетных документов, применяемых организацией (за исключением организаций государственного сектора), должен определять руководитель организации (ч. 4 ст. 9 Федерального закона от 06.12.2011 N 402-ФЗ «О бухгалтерском учете» (далее — Закон N 402-ФЗ). При этом организация может продолжать применять унифицированные формы, при необходимости изменив их с учетом требований ст. 9 Закона N 402-ФЗ, закрепив это в учетной политике (п. 4 ПБУ 1/2008 «Учетная политика организации»). Закон N 402-ФЗ не предусматривает обязательного применения форм первичных учетных документов, которые содержатся в альбомах унифицированных форм.
12.2012 N ПЗ-10/2012), а формы первичных учетных документов, применяемых организацией (за исключением организаций государственного сектора), должен определять руководитель организации (ч. 4 ст. 9 Федерального закона от 06.12.2011 N 402-ФЗ «О бухгалтерском учете» (далее — Закон N 402-ФЗ). При этом организация может продолжать применять унифицированные формы, при необходимости изменив их с учетом требований ст. 9 Закона N 402-ФЗ, закрепив это в учетной политике (п. 4 ПБУ 1/2008 «Учетная политика организации»). Закон N 402-ФЗ не предусматривает обязательного применения форм первичных учетных документов, которые содержатся в альбомах унифицированных форм.
В случае, если доставку товаров покупателю осуществляет перевозчик (сторонняя организация) на основании заключенного с покупателем договора перевозки, следует составлять транспортную накладную. Необходимость оформления транспортной накладной при перевозке грузов установлена ст. 8 Федерального закона от 08.11.2007 N 259-ФЗ «Устав автомобильного транспорта и городского наземного электрического транспорта» (далее — Устав) и п.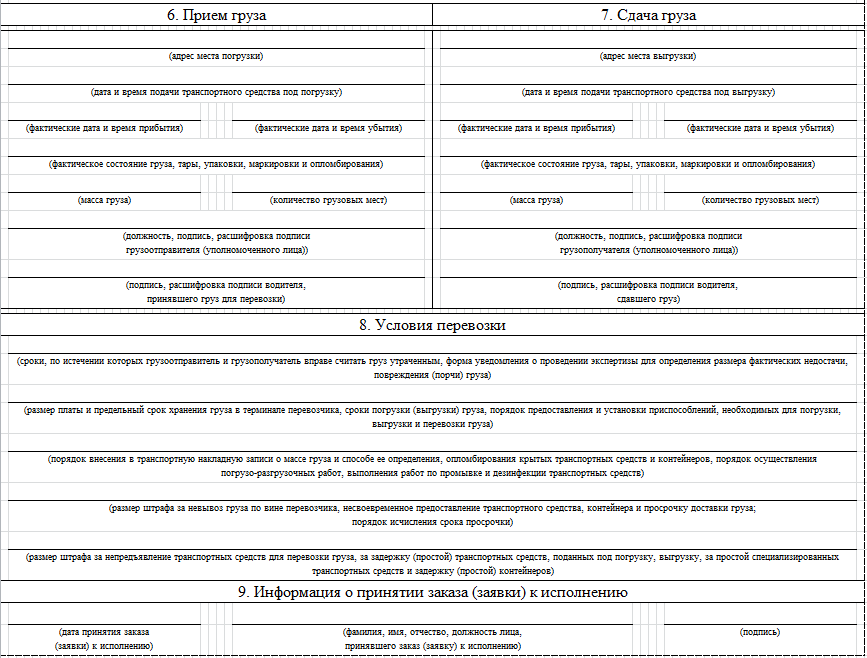 6 Правил (смотрите также письмо Минфина России от 28.01.2013 N 03-03-06/1/36). Транспортная накладная, если иное не предусмотрено договором перевозки груза, составляется грузоотправителем. Форма и порядок заполнения транспортной накладной устанавливаются Правилами.
6 Правил (смотрите также письмо Минфина России от 28.01.2013 N 03-03-06/1/36). Транспортная накладная, если иное не предусмотрено договором перевозки груза, составляется грузоотправителем. Форма и порядок заполнения транспортной накладной устанавливаются Правилами.
Однако в рассматриваемом случае организация сама перевозит продукцию, поэтому составление транспортной накладной не является обязательным.
Из Указаний по применению и заполнению форм, утвержденных Постановлением N 78 (далее — Указания), ТТН предназначена для учета движения товарно-материальных ценностей и расчетов грузоотправителей или грузополучателей с организациями (владельцами автотранспорта) за оказанные им услуги по перевозке грузов автомобильным транспортом. Указания содержат лишь общие рекомендации по заполнению ТТН. Порядок заполнения строки «Пункт погрузки» в них не освещен.
Согласно ст. 2 Устава грузоотправителем именуется физическое или юридическое лицо, которое по договору перевозки груза выступает от своего имени или от имени владельца груза и указывается в транспортной накладной. То есть ТТН выписывает лицо, которое является стороной договора перевозки груза (смотрите также письмо УФНС России по г. Москве от 30.12.2009 N 16-15/139277).
То есть ТТН выписывает лицо, которое является стороной договора перевозки груза (смотрите также письмо УФНС России по г. Москве от 30.12.2009 N 16-15/139277).
Таким образом, в строке «Грузоотправитель» ТНН указываются данные владельца груза либо лица, действующего от его имени. Согласно п. 2 ст. 54 ГК РФ место нахождения юридического лица определяется местом его государственной регистрации. Соответственно, в рассматриваемой строке должен быть указан юридический адрес грузоотправителя.
Что касается заполнения строки «Пункт погрузки», то в данной строке отражается не юридический адрес грузоотправителя, а фактический адрес места погрузки товара.
Отметим, что данные об адресе в строках «Грузоотправитель» и «Пункт погрузки» могут совпадать только в том случае, если фактически товар отгружается с территории, являющейся местом регистрации организации-грузоотправителя. Если же товар отгружается, например, со склада, принадлежащего грузоотправителю, но расположенного на иной территории, нежели он сам, данные в рассматриваемых строках совпадать не будут.
Для подтверждения сделанных выводов можно обратиться к Инструкции о порядке расчетов за перевозки грузов автомобильным транспортом (далее — Инструкция), утвержденной Минфином СССР, Госбанком СССР, ЦСУ при Совете Министров СССР, Минтрансом РСФСР 30.11.1983 NN 156, 30, 354/7, 10/998 (относится к старой форме ТТН, но порядок заполнения, установленный Инструкцией, может применяться к действующей форме ТТН с поправками на те строки и графы, которые были изменены). В Приложении N 3 к Инструкции приведен Порядок изготовления, учета и заполнения товарно-транспортных накладных на перевозку грузов автомобильным транспортом. В соответствии с п. 9 данного приложения в заголовочной части ТТН следует, в частности:
— в строках «Грузоотправитель» и «Грузополучатель» записать наименования организаций, производящих, соответственно, отгрузку (списание) и получение (оприходование) перечисленных в документе товарно-материальных ценностей;
— в строках «Пункт погрузки» и «Пункт разгрузки» записать адреса соответственно пунктов погрузки и разгрузки.
В рассматриваемой ситуации организация самостоятельно доставляет заказчику продукцию со склада поставщика, поэтому у поставщика, в принципе, отсутствует необходимость составления товарно-транспортных накладных. В данном случае поставщик исполняет свои обязательства перед покупателем (организацией) с момента подписания на своей территории товарной накладной (ТОРГ-12), передав продукцию представителю покупателя. В подтверждение данных слов можно привести постановления ФАС Северо-Кавказского округа от 20.05.2013 N Ф08-1853/13 по делу N А32-24456/2010, ФАС Московского округа от 24.12.2010 N Ф05-14841/10 по делу N А40-139282/2009, от 17.04.2007 N КА-А40/2560-07, Седьмого арбитражного апелляционного суда от 29.08.2011 N 07АП-6619/11. Согласен с такой позицией и Минфин России: смотрите, например, письма от 02.09.2011 N 03-03-06/1/540 и от 17.08.2011 N 03-03-06/1/500.
С учетом норм ст. 458 ГК РФ в случае получения покупателем товара в месте нахождения поставщика (на условиях самовывоза) за организацию перевозки отвечает сам покупатель, а не поставщик, если иное предусмотрено условиями заключенного договора, то есть грузоотправителем является покупатель.
В связи с этим, по нашему мнению, в рассматриваемом случае организации необходимо самостоятельно составить ТТН, в которой она будет выступать в роли грузоотправителя, а заказчик — в роли грузополучателя. В строке «Пункт погрузки» следует указывать адрес склада (т.е. производственной площадки поставщика в Вологодской области), с которого фактически происходит отгрузка продукции.
В подтверждение сказанного приведем постановление Восемнадцатого арбитражного апелляционного суда от 27.06.2013 N 18АП-5437/13. Судьи указали, что по общему правилу ТТН составляется отправителем груза. ООО по отношению к товарам, вывозимым самовывозом, либо по товарам, которые доставлялись посредством грузоперевозчиков, является собственником, следовательно, если товар вывезен со склада поставщика покупателем самовывозом при условии перехода права собственности в момент передачи товара покупателю, товаросопроводительным документом является товарная накладная по форме ТОРГ-12. В данном случае поставщик обязан составить только накладную по форме ТОРГ-12, так как он никаких дополнительных договоров не заключает, в его обязанности входят лишь подготовка товара к отгрузке и извещение об этом покупателя.
При этом суды указывают, что НК РФ не содержит требования об обязательном заполнении всех граф унифицированных форм бухгалтерских документов и отдельные нарушения не могут служить основанием для отказа в принятии к учету таких документов, поскольку они не свидетельствуют об отсутствии затрат, а выявленные недостатки в оформлении первичных документов контрагентами не препятствуют установлению факта осуществления расходов, не отменяют их документального подтверждения и производственной направленности (постановления ФАС Северо-Западного округа от 12.
По мнению Минфина России, выраженному в письме от 04.02.2015 N 03-03-10/4547, ошибки в первичных учетных документах, не препятствующие налоговым органам при проведении налоговой проверки идентифицировать продавца, покупателя товаров (работ, услуг), имущественных прав, наименование товаров (работ, услуг), имущественных прав, их стоимость и другие обстоятельства документируемого факта хозяйственной жизни, обуславливающие применение соответствующего порядка налогообложения, не являются основанием для отказа в принятии соответствующих расходов в уменьшение налоговой базы по налогу на прибыль.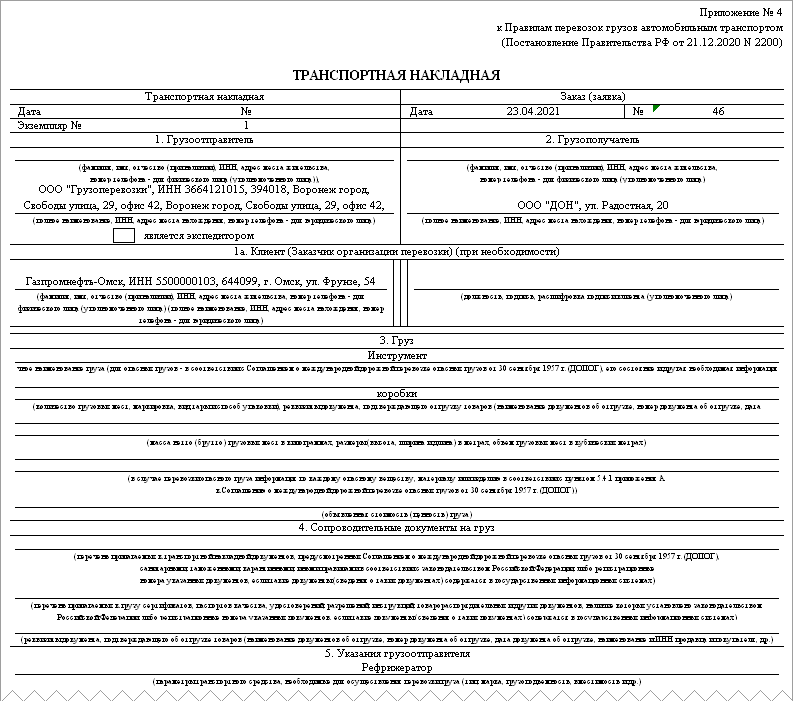
В связи с этим считаем, что даже неправильное заполнение строки «Пункт погрузки» не должно создавать существенных налоговых рисков для организации при условии подтверждения реальности хозяйственных операций другими документами.
Ответ подготовил:
Эксперт службы Правового консалтинга ГАРАНТ
аудитор, член РКА Буланцов Михаил
Контроль качества ответа:
Рецензент службы Правового консалтинга ГАРАНТ
аудитор, член РСА Горностаев Вячеслав
Кто должен оформлять накладную 1-Т?
Получить консультацию
Ответ
Согласно Письму Министерства финансов Российской Федерации от 17.08.2011 года №03-03-06/1/499 в соответствии со статьей 2 Федерального закона от 8 ноября 2007 г. N 259-ФЗ «Устав автомобильного транспорта и городского наземного электрического транспорта» транспортная накладная — перевозочный документ, подтверждающий заключение договора перевозки груза.
Форма и порядок заполнения транспортной накладной установлены Правилами перевозки грузов автомобильным транспортом, утвержденными Постановлением Правительства Российской Федерации от 15 апреля 2011 г. N 272 (далее — Правила перевозки грузов).
Одновременно продолжают действовать «Общие правила перевозки грузов автомобильным транспортом», утвержденные Минавтотрансом РСФСР 30.07.1971, в соответствии с которыми основным документом, предназначенным для учета движения товарно-материальных ценностей и расчетов за их перевозки автомобильным транспортом, является товарно-транспортная накладная.
Форма товарно-транспортной накладной (форма N 1-Т) утверждена Постановлением Госкомстата России от 28 ноября 1997 г. N 78.
Постановлением Госкомстата России от 25.12.1998 N 132 «Об утверждении унифицированных форм первичной учетной документации по учету торговых операций» утверждена товарная накладная (форма N ТОРГ-12), она относится к первичной учетной документации по учету торговых операций и применяется для оформления продажи (отпуска) товарно-материальных ценностей сторонней организации.
В этой связи использование транспортной накладной не исключает также и применение накладных форм N 1-Т и ТОРГ-12.
При этом в утвержденной Правилами перевозки грузов форме транспортной накладной содержатся все необходимые сведения о перевозчике, грузоотправителе, грузополучателе, условиях перевозки груза, а также данные, подтверждающие факт транспортировки груза и затраты на такую перевозку.
В соответствии с пунктом 1 статьи 252 Налогового кодекса Российской Федерации расходами признаются обоснованные и оформленные в соответствии с законодательством Российской Федерации затраты, понесенные налогоплательщиком.
Таким образом, в случае наличия договора перевозки груза, подтверждение затрат организации на перевозку груза автомобильным транспортом и факта его транспортировки осуществляется на основании как транспортной накладной, так и накладной формы N 1-Т, используемой в бухгалтерском и налоговом учете.
Если между Вашей организацией и транспортными компаниями заключен договор перевозки грузов, то накладная №1-Т или транспортная накладная заполняется Вашей организацией и подтверждает заключение договора перевозки груза.
Если договорные отношения между Вашей организацией и транспортной компанией отсутствуют, следовательно, доставка товара до склада транспортной компании это разовое оказание услуг, выполнение которых подтверждается актами выполненных работ.
Данный вывод находит свое отражение в существующей судебной практике например, согласно Определению ВАС РФ от 31.08.2010 № ВАС-11597/10 в соответствии с пунктом 1 статьи 779 и пунктом 1 статьи 781 Гражданского кодекса Российской Федерации (далее — Кодекс) по договору возмездного оказания услуг исполнитель обязуется по заданию заказчика оказать услуги (совершить определенные действия или осуществить определенную деятельность), а заказчик обязуется оплатить эти услуги в сроки и в порядке, которые указаны в договоре возмездного оказания услуг.
Удовлетворяя исковые требования, суды исходили из того, что факт оказания услуг подтвержден надлежащими актами. Доказательств оплаты оказанных услуг ответчиком не представлено. Судами отмечено, что доказательства, свидетельствующие о заключении между сторонами договоров перевозки, отсутствуют, в связи с чем оснований для применения к рассматриваемой ситуации положений главы 40 Кодекса не имеется.
То есть, Вы может оформлять с транспортными организациями именно акты выполненных работ, а не транспортные накладные или накладные №1-Т. В этом случае к отношениям сторон будут применяться положения главы 39 ГК РФ, а не главы 40 ГК РФ.
26.01.2012
Юрист Тихонова А.А.
Электронная конфигурация — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 1701
Электронная конфигурация атомного вида (нейтрального или ионного) позволяет нам понять форму и энергию его электронов. Многие общие правила принимаются во внимание при назначении «местоположения» электрона его предполагаемому энергетическому состоянию, однако эти присвоения произвольны, и всегда неясно, какой электрон описывается. Знание электронной конфигурации вида дает нам лучшее понимание его связывающей способности, магнетизма и других химических свойств.
Знание электронной конфигурации вида дает нам лучшее понимание его связывающей способности, магнетизма и других химических свойств.
Введение
Электронная конфигурация является стандартной записью, используемой для описания электронной структуры атома. В орбитальном приближении мы позволяем каждому электрону занимать орбиталь, которая может быть решена одной волновой функцией. При этом мы получаем три квантовых числа (n, l , m l ), которые совпадают с числами, полученными из решения уравнения Шредингера для атома водорода Бора. Следовательно, многие из правил, которые мы используем для описания адреса электрона в атоме водорода, также можно использовать в системах, включающих несколько электронов. При назначении электронов орбиталям мы должны следовать набору из трех правил: принципу Ауфбау, принципу исключения Паули и правилу Хунда.
Волновая функция является решением уравнения Шредингера. Решая уравнение Шредингера для атома водорода, мы получаем три квантовых числа, а именно главное квантовое число (n), квантовое число орбитального углового момента ( l ) и магнитное квантовое число (m l ). Существует четвертое квантовое число, называемое спиновым магнитным квантовым числом (m s ), которое не получается из решения уравнения Шредингера. Вместе эти четыре квантовых числа можно использовать для описания местоположения электрона в атоме водорода Бора. Эти числа можно рассматривать как «адрес» электрона в атоме.
Существует четвертое квантовое число, называемое спиновым магнитным квантовым числом (m s ), которое не получается из решения уравнения Шредингера. Вместе эти четыре квантовых числа можно использовать для описания местоположения электрона в атоме водорода Бора. Эти числа можно рассматривать как «адрес» электрона в атоме.
Обозначение
Чтобы помочь описать подходящее обозначение для электронной конфигурации, лучше всего сделать это на примере. В этом примере мы будем использовать атом йода. There are two ways in which electron configuration can be written:
I: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 4d 10 5p 5
или
I: [Kr]5s 2 4d 10 5p 5
В обоих этих типах обозначений порядок энергетических уровней должен быть записан в виде увеличения энергии, показывая число электронов в каждой подоболочке в виде показателя степени.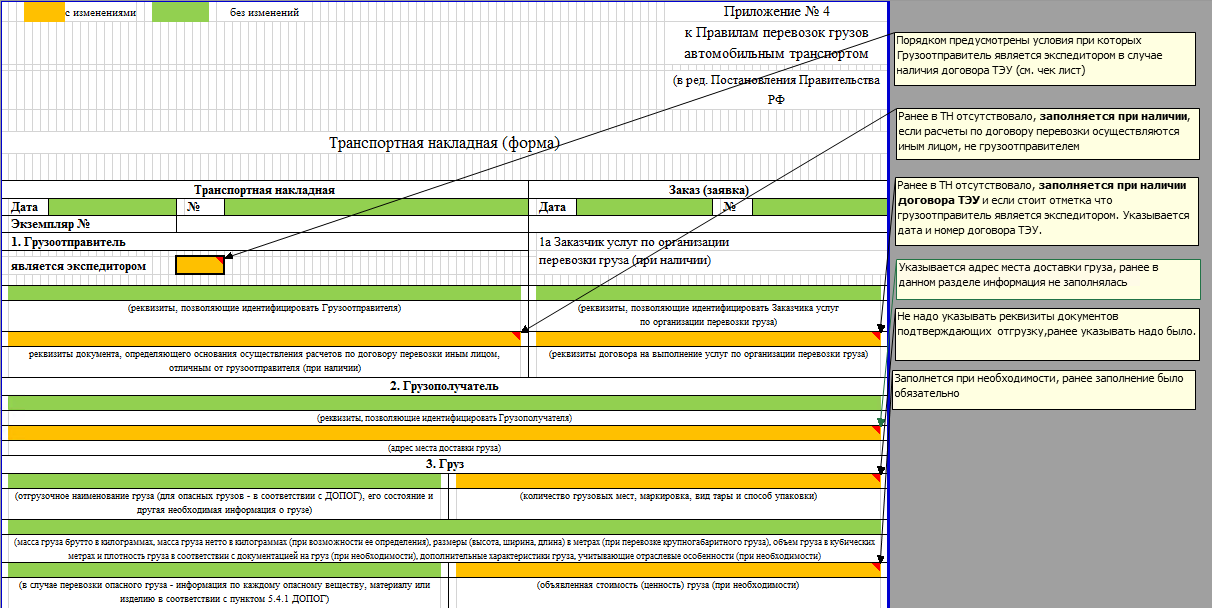 В краткой записи вы заключаете в скобки элемент благородного газа , предшествующий , за которым следует конфигурация электрона валентной оболочки. Периодическая таблица показывает, что кирптон (Kr) является предыдущим благородным газом, указанным перед йодом. Конфигурация благородного газа охватывает энергетические состояния ниже, чем электроны валентной оболочки. Следовательно, в данном случае [Kr]=1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p
В краткой записи вы заключаете в скобки элемент благородного газа , предшествующий , за которым следует конфигурация электрона валентной оболочки. Периодическая таблица показывает, что кирптон (Kr) является предыдущим благородным газом, указанным перед йодом. Конфигурация благородного газа охватывает энергетические состояния ниже, чем электроны валентной оболочки. Следовательно, в данном случае [Kr]=1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p
Квантовые числа
Главное квантовое число (n)
Главное квантовое число n указывает на оболочку или энергетический уровень, на котором находится электрон. Значение n может быть установлено от 1 до n , где n — это значение самой внешней оболочки, содержащей электрон. Это квантовое число может быть только положительным, ненулевым и целым числом. то есть n =1,2,3,4,..
Например, атом йода имеет крайние электроны на 5р-орбитали. Следовательно, основное квантовое число для йода равно 5.
Квантовое число орбитального углового момента (
l )Квантовое число орбитального углового момента, l , указывает подоболочку электрона. Вы также можете определить форму атомной орбитали с помощью этого квантового числа. Подоболочка s соответствует l = 0, a p 9Подоболочка 0033 = 1, подоболочка d = 2, подоболочка f = 3 и так далее. Это квантовое число может принимать только положительные и целые значения, хотя может принимать и нулевое значение. В общем, для каждого значения n существует n значений l . Кроме того, значение l находится в диапазоне от 0 до n-1. Например, если n=3, l =0,1,2.
Итак, что касается примера, использованного выше, значения l йода для n = 5 равны l = 0, 1, 2, 3, 4.
Магнитное квантовое число (m
l ) Магнитное квантовое число m l представляет орбитали данной подоболочки. Для данного l m l может варьироваться от -l до +l . Подоболочка p ( l = 1), например, может иметь три орбитали, соответствующие m l = -1, 0, +1. Другими словами, он определяет орбитали p x , p y и p z подоболочки p. (Однако m l числа не обязательно соответствуют данной орбитали. Тот факт, что существует три орбитали, просто указывает на три орбитали p-подоболочки.) В общем, для данного l существует 2 l +1 возможных значений для m l ; а в основной оболочке n на этом энергетическом уровне находится n 2 орбиталей.
Для данного l m l может варьироваться от -l до +l . Подоболочка p ( l = 1), например, может иметь три орбитали, соответствующие m l = -1, 0, +1. Другими словами, он определяет орбитали p x , p y и p z подоболочки p. (Однако m l числа не обязательно соответствуют данной орбитали. Тот факт, что существует три орбитали, просто указывает на три орбитали p-подоболочки.) В общем, для данного l существует 2 l +1 возможных значений для m l ; а в основной оболочке n на этом энергетическом уровне находится n 2 орбиталей.
Продолжая пример выше, значения m l йода равны m l = -4, -3, -2, -1, 0 1, 2, 3, 4. Они произвольно соответствуют 5s, 5p x , 5p y , 5p z , 4d x 2 -y 2 , 4d z 2 , 4d xy , 4d xz и 4d yz 5 орбиталей.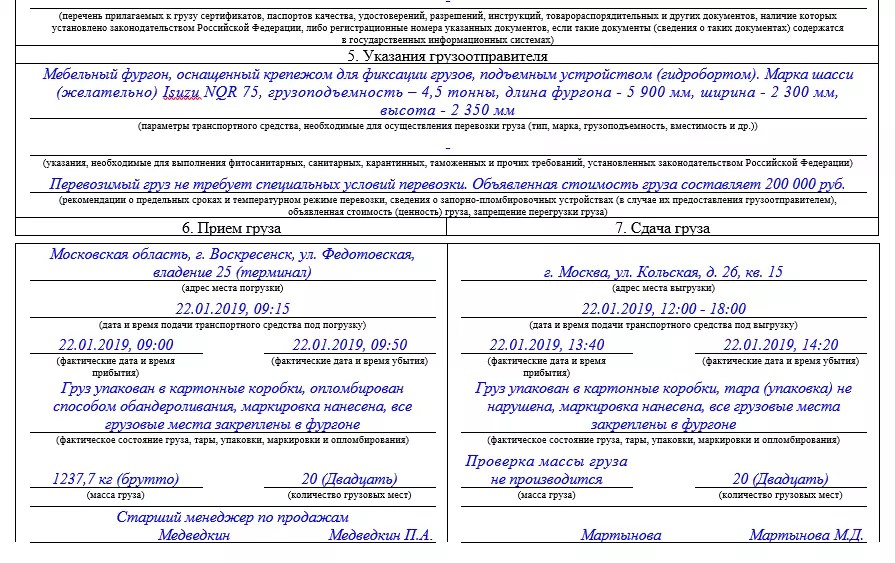
Спиновое магнитное квантовое число (m
s )Спиновое магнитное квантовое число может иметь значение только +1/2 или -1/2. Значение 1/2 — это спиновое квантовое число s, которое описывает спин электрона. Благодаря вращению электрона создается магнитное поле. В общем случае электрон с m s =+1/2 называется альфа-электроном, а тот, у которого m s =-1/2, называется бета-электроном. Никакие два спаренных электрона не могут иметь одинаковое значение спина.
Однако Бор предположил, что из этих четырех квантовых чисел только главное квантовое число n определяет энергию электрона. Следовательно, 3s-орбиталь ( l = 0) имеет ту же энергию, что и 3p ( l = 1) и 3d ( l = 2) орбитали, независимо от разницы в значениях l . Однако этот постулат верен только для атома водорода Бора или других водородоподобных атомов.
Имея дело с многоэлектронными системами, мы должны учитывать электрон-электронные взаимодействия. Следовательно, ранее описанный постулат нарушается в том смысле, что энергия электрона теперь определяется как главным квантовым числом n, так и квантовым числом орбитального углового момента l . Хотя уравнение Шредингера для многоэлектронных атомов чрезвычайно сложно решить математически, мы все же можем описать их электронные структуры через электронные конфигурации.
Следовательно, ранее описанный постулат нарушается в том смысле, что энергия электрона теперь определяется как главным квантовым числом n, так и квантовым числом орбитального углового момента l . Хотя уравнение Шредингера для многоэлектронных атомов чрезвычайно сложно решить математически, мы все же можем описать их электронные структуры через электронные конфигурации.
Общие правила электронной конфигурации
Существует набор общих правил, которые используются для определения электронной конфигурации атомных видов: принцип Ауфбау, правило Хунда и принцип исключения Паули. Прежде чем продолжить, важно понять, что каждая орбиталь может быть занята двумя электронами с противоположным спином (что будет обсуждаться позже). В следующей таблице показано возможных числа электронов, которые могут занимать каждую орбиталь в данной подоболочке.
| подоболочка | количество орбиталей | общее количество возможных электронов на каждой орбитали |
| с | 1 | 2 |
| р | 3 (p x , p y , p z ) | 6 |
| д | 5 (D x 2 — Y 2 , D Z 2 , D XY , D XZ , D YZ ) | 10 |
| ф | 7 (F Z 3 , F XZ 2 , F XYZ , F x (X 2 -3Y 2 ) , F ), , F ), , F ). f z(x 2 -y 2 ) , f г(3x 2 -у 2 ) f z(x 2 -y 2 ) , f г(3x 2 -у 2 ) | 14 |
Используя наш пример, йод, опять же, мы видим в периодической таблице, что его атомный номер равен 53 (это означает, что он содержит 53 электрона в нейтральном состоянии). Полная конфигурация электронов — 1S 2 2S 2 2P 6 3S 2 3P 6 4S 2 3D 10 4P 6 5S 2 4D 4P 6 5S 2 4D 4P 6 5S 2 4D 0050 10 5p 5 . Если вы подсчитаете все эти электроны, вы увидите, что в сумме получается 53 электрона. Обратите внимание, что каждая подоболочка может содержать только максимальное количество электронов, как указано в таблице выше.
Aufbau Principle
Слово «Aufbau» в переводе с немецкого означает «наращивание». Принцип Ауфбау, также называемый принципом нарастания, гласит, что электроны занимают орбитали в порядке возрастания энергии. Порядок занятия следующий:
Принцип Ауфбау, также называемый принципом нарастания, гласит, что электроны занимают орбитали в порядке возрастания энергии. Порядок занятия следующий:
1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p 9Рисунок 1. однако есть исключения, такие как медь
и хром.
Этот порядок заполнения приблизительно соответствует возрастанию энергетического уровня орбиталей. Следовательно, электроны занимают орбитали таким образом, что энергия остается минимальной. То есть подоболочки 7s, 5f, 6d, 7p не будут заполнены электронами, если орбитали с более низкой энергией, от 1s до 6p, уже полностью заняты. Кроме того, важно отметить, что, хотя математически было показано, что энергия 3d-орбитали ниже, чем у 4s-орбитали, электроны сначала занимают 4s-орбиталь, а затем 3d-орбиталь. Это наблюдение можно объяснить тем фактом, что 3d-электроны с большей вероятностью находятся ближе к ядру; следовательно, они сильнее отталкивают друг друга. Тем не менее, запоминание порядка орбитальных энергий и, следовательно, отнесение электронов к орбиталям может стать довольно простым, когда речь идет о периодической таблице.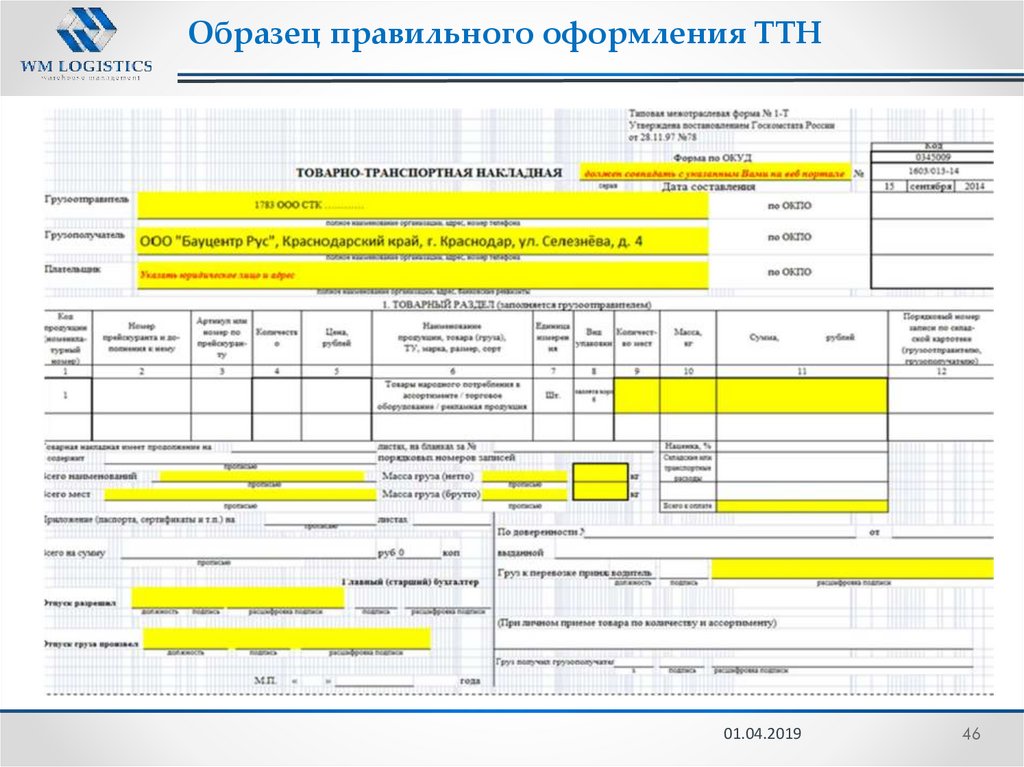
Чтобы понять этот принцип, давайте рассмотрим атом брома. Бром (Z = 35), который имеет 35 электронов, можно найти в периоде 4, группе VII периодической таблицы. Поскольку бром имеет 7 валентных электронов, 4s-орбиталь будет полностью заполнена 2 электронами, а оставшиеся пять электронов займут 4p-орбиталь. Таким образом, полная или расширенная электронная конфигурация брома в соответствии с принципом Ауфбау выглядит следующим образом:0050 6 4с 2 3д 10 4п 5 . Если мы добавим показатели степени, мы получим в общей сложности 35 электронов, что подтверждает правильность наших обозначений.
Правило Хунда
Правило Хунда гласит, что когда электроны занимают вырожденные орбитали (т.е. те же самые n и l квантовые числа), они должны сначала занять пустые орбитали, прежде чем занять их дважды. Кроме того, наиболее стабильная конфигурация возникает, когда спины параллельны (т. Е. Все альфа-электроны или все бета-электроны). Азот, например, имеет 3 электрона, занимающих 2р-орбиталь. Согласно правилу Хунда, они должны сначала занять каждую из трех вырожденных p-орбиталей, а именно 2p x орбиталь, 2p y орбиталь и 2p z орбиталь, и с параллельными спинами (рис. 2). Конфигурация ниже неверна, потому что третий электрон занимает не занимает пустую орбиталь 2p z . Вместо этого он занимает наполовину заполненную орбиталь 2p x . Следовательно, это нарушение правила Хунда (рис. 2).
Азот, например, имеет 3 электрона, занимающих 2р-орбиталь. Согласно правилу Хунда, они должны сначала занять каждую из трех вырожденных p-орбиталей, а именно 2p x орбиталь, 2p y орбиталь и 2p z орбиталь, и с параллельными спинами (рис. 2). Конфигурация ниже неверна, потому что третий электрон занимает не занимает пустую орбиталь 2p z . Вместо этого он занимает наполовину заполненную орбиталь 2p x . Следовательно, это нарушение правила Хунда (рис. 2).
Рис. 2. Наглядное представление принципа Ауфбау и правила Хунда. Отметим, что заполнение электронами каждой орбитали
(p x , p y и p z ) является произвольным до тех пор, пока электроны заполняются по отдельности, прежде чем два электрона займут одну и ту же орбиталь.
(a)Эта диаграмма представляет правильное заполнение электронами атома азота. (b) Эта диаграмма представляет неправильное
заполнение электронами атома азота.
Принцип исключения Паули
Вольфганг Паули постулировал, что каждый электрон можно описать уникальным набором из четырех квантовых чисел. Следовательно, если два электрона занимают одну и ту же орбиталь, например, 3s-орбиталь, их спины должны быть спаренными. Хотя они имеют одно и то же главное квантовое число (n=3), одинаковое квантовое число орбитального углового момента (l=0) и одно и то же магнитное квантовое число (m l =0), они имеют разные спиновые магнитные квантовые числа (m s =+1/2 и m s =-1/2).
Электронные конфигурации катионов и анионов
То, как мы обозначаем электронные конфигурации катионов и анионов, в основном аналогично тому, как мы обозначаем нейтральные атомы в их основном состоянии. То есть мы следуем трем важным правилам: принципу Ауфбау, принципу исключения Паули и правилу Хунда. Электронная конфигурация катионов определяется путем удаления электронов сначала с самой внешней p-орбитали, затем с s-орбитали и, наконец, с d-орбитали (если необходимо удалить еще какие-либо электроны). Например, электронная конфигурация кальция в основном состоянии (Z=20) равна 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 . Однако ион кальция (Ca 2+ ) имеет на два электрона меньше. Следовательно, электронная конфигурация для Ca 2+ имеет вид 1s 2 2s 2 2p 6 3s 2 3p 6 . Поскольку нам нужно убрать два электрона, мы сначала удаляем электроны с самой внешней оболочки (n=4). В этом случае все подоболочки 4p пусты; следовательно, мы начинаем с удаления с s-орбитали, которая является 4s-орбиталью. Электронная конфигурация для Ca 2+ такое же, как у аргона, имеющего 18 электронов. Следовательно, мы можем сказать, что оба изоэлектронны.
Например, электронная конфигурация кальция в основном состоянии (Z=20) равна 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 . Однако ион кальция (Ca 2+ ) имеет на два электрона меньше. Следовательно, электронная конфигурация для Ca 2+ имеет вид 1s 2 2s 2 2p 6 3s 2 3p 6 . Поскольку нам нужно убрать два электрона, мы сначала удаляем электроны с самой внешней оболочки (n=4). В этом случае все подоболочки 4p пусты; следовательно, мы начинаем с удаления с s-орбитали, которая является 4s-орбиталью. Электронная конфигурация для Ca 2+ такое же, как у аргона, имеющего 18 электронов. Следовательно, мы можем сказать, что оба изоэлектронны.
Электронная конфигурация анионов определяется добавлением электронов в соответствии с принципом Ауфбау. Мы добавляем электроны, чтобы заполнить крайнюю занятую орбиталь, а затем добавляем электроны на следующую более высокую орбиталь. Нейтральный атом хлора (Z=17), например, имеет 17 электронов. Следовательно, его электронная конфигурация в основном состоянии может быть записана как 1s 2 2s 2 2p 6 3s 2 3p 5 . Ион хлорида (Cl —), с другой стороны, имеет дополнительный электрон, всего 18 электронов. Следуя принципу Ауфбау, электрон сначала занимает частично заполненную подоболочку 3p, делая 3p-орбиталь полностью заполненной. Таким образом, электронная конфигурация для Cl — может быть обозначена как 1s 2 2s 2 2p 6 3s 2 3p 6 . Опять же, электронная конфигурация для иона хлорида такая же, как у Ca 2+ и Аргон. Следовательно, все они изоэлектронны друг другу.
Нейтральный атом хлора (Z=17), например, имеет 17 электронов. Следовательно, его электронная конфигурация в основном состоянии может быть записана как 1s 2 2s 2 2p 6 3s 2 3p 5 . Ион хлорида (Cl —), с другой стороны, имеет дополнительный электрон, всего 18 электронов. Следуя принципу Ауфбау, электрон сначала занимает частично заполненную подоболочку 3p, делая 3p-орбиталь полностью заполненной. Таким образом, электронная конфигурация для Cl — может быть обозначена как 1s 2 2s 2 2p 6 3s 2 3p 6 . Опять же, электронная конфигурация для иона хлорида такая же, как у Ca 2+ и Аргон. Следовательно, все они изоэлектронны друг другу.
Задачи
1. Какой из объясненных выше принципов говорит нам о том, что спаренные электроны не могут иметь одинаковое значение спина?
2. Найдите значения n, l , m l и m s для следующего:
a. мг
мг
б. Га
в. Co
3. Какова возможная комбинация квантовых чисел 5d-орбитали? Приведите пример элемента, у которого орбиталь 5d является самой внешней орбиталью.
4. Что из следующего не может существовать (может быть более одного ответа):
a. п = 4; л = 4; м л = -2; м с = +1/2
б. п = 3; л = 2; м л = 1; м с = 1
в. п = 4; л = 3; м л = 0; м с = +1/2
д. п = 1; л = 0; м л = 0; м с = +1/2
е. п = 0; л = 0; м л = 0; m s = +1/2
5. Напишите электронные конфигурации для следующего:
a. Р
б. S 2-
в. Zn 3+
Ответы
1. Принцип исключения Паули
2. а. п = 3; л = 0, 1, 2; m l = -2, -1, 0, 1, 2; m s может быть +1/2 или -1/2
b. п = 4; л = 0, 1, 2, 3; m l = -3, -2, -1, 0, 1, 2, 3; m s может принимать значения +1/2 или -1/2
п = 4; л = 0, 1, 2, 3; m l = -3, -2, -1, 0, 1, 2, 3; m s может принимать значения +1/2 или -1/2
в. п = 3; л = 0, 1, 2; m l = -2, -1, 0, 1, 2, 3; m s может принимать значения +1/2 или -1/2
3. n = 5; л = 3; м л = 0; м с = +1/2. Например, осмий (Os).
4. а. Значение l не может быть равно 4, потому что l находится в диапазоне (0 — n-1)
b. m s может быть только +1/2 или -1/2
c. Хорошо
д. Хорошо
эл. Значение n не может быть равно нулю.
5. а. 1s 2 2s 2 2p 6 3s 2 3p 3
b. 1s 2 2s 2 2p 6 3s 2 3p 6
c. 1S 2 2S 2 2P 6 3S 2 3P 6 4S 2 3D 7
СПИСАВ
- ATKINS, P.
 W. & De Paula, J. 2006). Физическая химия для наук о жизни. Нью-Йорк, штат Нью-Йорк: WH Freeman and Company.
W. & De Paula, J. 2006). Физическая химия для наук о жизни. Нью-Йорк, штат Нью-Йорк: WH Freeman and Company. - Петруччи, Р. Х., Харвуд, В. С., и Херринг, Ф. Г. (2002). Общая химия: принципы и современные приложения. Река Аппер-Сэдл, Нью-Джерси: Prentice-Hall, Inc.
- Шагури, Ричард. Химия 1A Лекционный сборник. 4-е изд. Пользовательская публикация. 2006. Печать
Авторы и ссылки
- Ланна Луа, Эндрю Искандар (Калифорнийский университет в Дэвисе, бакалавриат) Мэри Магсомбол (Калифорнийский университет в Дэвисе)
Конфигурация Electron распространяется по недекларированной лицензии и была создана, изменена и/или курирована LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Показать страницу TOC
- № на стр.

- Теги
5.17: Правило Хунда и диаграммы орбитального заполнения
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 52975
Вы когда-нибудь задумывались, что означают эти знаки ограничения нагрузки на мосту?
Знак выше означает, что не допускается перевозка грузов весом более пяти тонн, поскольку это может повредить конструкцию. Есть ограничения на вес, который может выдержать мост, есть ограничения на количество людей, которые могут безопасно занимать комнату, и есть ограничения на то, что может попасть на электронную орбиту.
Есть ограничения на вес, который может выдержать мост, есть ограничения на количество людей, которые могут безопасно занимать комнату, и есть ограничения на то, что может попасть на электронную орбиту.
Правило Хунда
Последнее из трех правил построения расположения электронов требует, чтобы электроны размещались по одному на множестве орбиталей в пределах одного и того же подуровня. Это минимизирует естественные силы отталкивания, которые один электрон оказывает на другой. Правило Хунда гласит, что каждая орбиталь с одинаковой энергией занята одним электроном до того, как любая орбиталь будет занята вторым электроном, и что каждый из отдельных электронов должен иметь одинаковый спин. На рисунке ниже показано, как набор из трех \(p\)-орбиталей заполнен одним, двумя, тремя и четырьмя электронами.
Рисунок \(\PageIndex{2}\): Подуровень \(2p\) для элементов бор \(\left( Z=5 \right)\), углерод \(\left( Z=6 \right) \), азот \(\left( Z=7 \right)\) и кислород \(\left( Z=8 \right)\). Согласно правилу Хунда, когда электроны добавляются к набору орбиталей с одинаковой энергией, один электрон входит в каждую орбиталь до того, как любая орбиталь получит второй электрон. (Источник: Джой Шэн; Источник: Фонд CK-12; Лицензия: CC BY-NC 3.0 (открывается в новом окне))
Согласно правилу Хунда, когда электроны добавляются к набору орбиталей с одинаковой энергией, один электрон входит в каждую орбиталь до того, как любая орбиталь получит второй электрон. (Источник: Джой Шэн; Источник: Фонд CK-12; Лицензия: CC BY-NC 3.0 (открывается в новом окне))Схемы орбитального заполнения
An 9Диаграмма заполнения орбиты 0024 — это более наглядный способ представить расположение всех электронов в конкретном атоме. На диаграмме заполнения орбит отдельные орбитали показаны кружками (или квадратами), а орбитали внутри подуровня нарисованы рядом друг с другом по горизонтали. Каждый подуровень помечен своим главным энергетическим уровнем и подуровнем. Электроны указаны стрелками внутри кругов. Стрелка, указывающая вверх, указывает одно направление вращения, а стрелка, указывающая вниз, указывает другое направление. Диаграммы заполнения орбит водорода, гелия и лития показаны на рисунке ниже.
Рисунок \(\PageIndex{3}\): Диаграммы заполнения орбит для водорода, гелия и лития. (Источник: Джой Шэн; Источник: Фонд CK-12; Лицензия: CC BY-NC 3.0 (открывается в новом окне))
(Источник: Джой Шэн; Источник: Фонд CK-12; Лицензия: CC BY-NC 3.0 (открывается в новом окне))В соответствии с процессом Ауфбау подуровни и орбитали заполняются электронами в порядке возрастания энергии. Поскольку подуровень \(s\) состоит всего из одной орбитали, второй электрон просто спаривается с первым электроном, как в гелии. Следующим элементом является литий, и он требует использования следующего доступного подуровня, \(2s\).
Схема заполнения углем показана на рисунке ниже. У углерода есть два \(2p\) электрона, и каждый занимает свою \(2p\) орбиталь.
Рисунок \(\PageIndex{4}\): Диаграмма заполнения орбит углерода. (Источник: Joy Sheng; Источник: CK-12 Foundation; Лицензия: CC BY-NC 3.0(opens in new window))Кислород имеет четыре \(2p\) электрона. После того, как на каждой \(2p\)-орбитали будет один электрон, четвертый электрон может быть помещен на первую \(2p\)-орбиталь со спином, противоположным спину другого электрона на этой орбитали.
Рисунок \(\PageIndex{5}\): Диаграмма заполнения орбиты кислородом.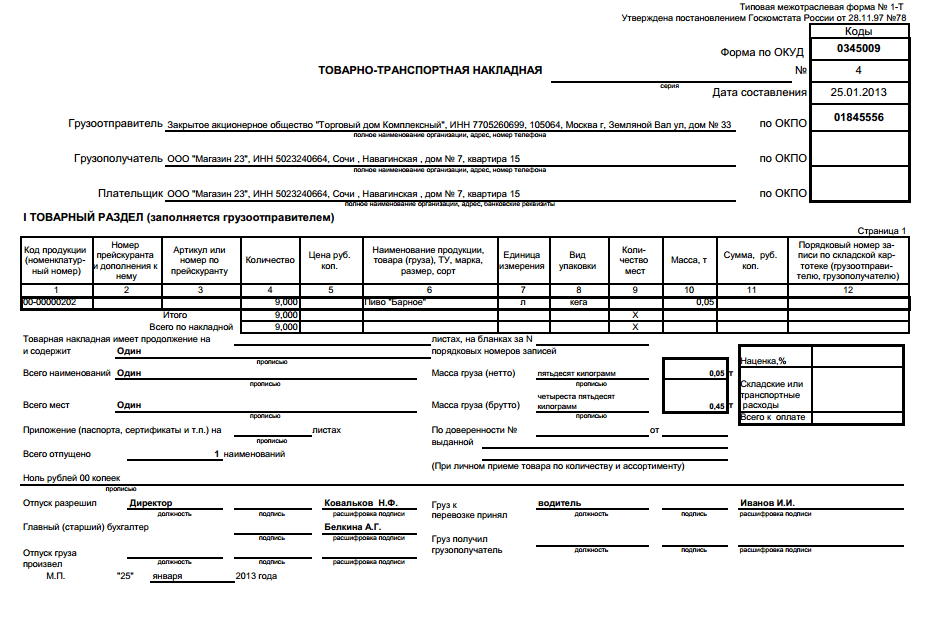 (Источник: Joy Sheng; Источник: CK-12 Foundation; Лицензия: CC BY-NC 3.0 (opens in new window))
(Источник: Joy Sheng; Источник: CK-12 Foundation; Лицензия: CC BY-NC 3.0 (opens in new window)) Резюме
- Правило Хунда определяет порядок заполнения электронами набора орбиталей.
- Диаграммы заполнения орбит — это способ указать местонахождение электронов на орбиталях.
Обзор
- Государственное правило Гунда.
- Что такое орбитальная диаграмма заполнения?
- Верна ли схема на рисунке ниже? Поясните свой ответ. Рисунок \(\PageIndex{6}\) (Источник: Джой Шэн; Источник: CK-12 Foundation; Лицензия: CC BY-NC 3.0 (откроется в новом окне))
- Верна ли схема на рисунке ниже? Поясните свой ответ. Рисунок \(\PageIndex{7}\) (Источник: Джой Шэн; Источник: CK-12 Foundation; Лицензия: CC BY-NC 3.0 (откроется в новом окне))
Эта страница под названием 5.


 W. & De Paula, J. 2006). Физическая химия для наук о жизни. Нью-Йорк, штат Нью-Йорк: WH Freeman and Company.
W. & De Paula, J. 2006). Физическая химия для наук о жизни. Нью-Йорк, штат Нью-Йорк: WH Freeman and Company.